英文原题:Total Synthesis and Stereochemical Assignment of Roselipin 1A
通讯作者:Tao Ye (叶涛),北京大学深圳研究生院
作者:Yangyang Jiang (蒋阳阳), Junyang Liu (刘君羊), Yian Guo (郭益安), and Tao Ye (叶涛)*
研究背景:
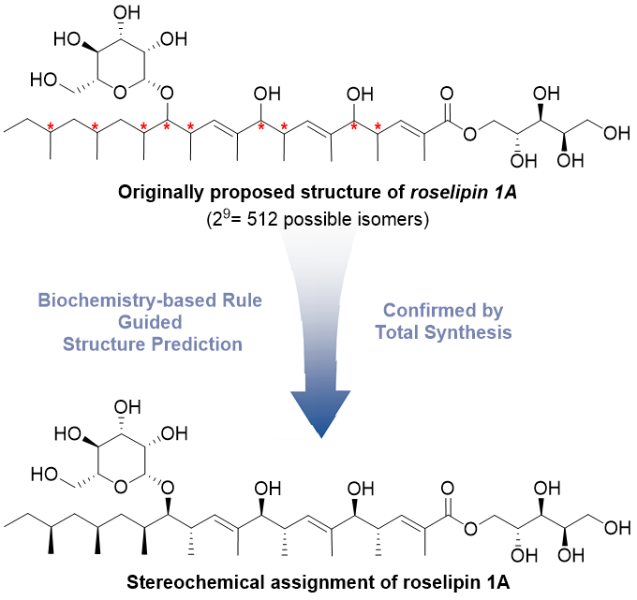
天然产物在新药和先导化合物的开发中起着重要作用,而准确无误地确定天然产物的立体结构信息则是其中关键一环。尽管已经发展了很多技术和方法(如NMR、HRMS、XRD和ECD等)用于确定天然产物结构信息,但是通过这些技术和方法得到的结果并不完全准确。通过全合成手段合成目标构型的样品并与天然分离的样品进行表征数据的比对仍是确定天然产物立体结构最准确可靠的方法之一。然而对于含有多个未知手性中心的天然产物来说,通过全合成手段来合成所有潜在的异构体显然是耗时耗力的,而可靠的结构预测规则可以帮助合成化学家排除一些潜在的异构体从而缩小范围。Roselipins是由2015年诺贝尔生理学或医学奖获得者Ōmura的课题组于1999年从海洋真菌Gliocladium roseum KF-1040的培养液中提取到的一类糖脂类天然产物,其家族分子的结构如图1所示。该课题组确定了该家族所有分子的二维平面结构,均由一个聚酮单元和两个糖基单元组成,其中聚酮单元的9个手性中心的相对、绝对立体化学并没有得到确定,以该家族的roselipin 1A为例,其潜在的异构体数量高达512种。
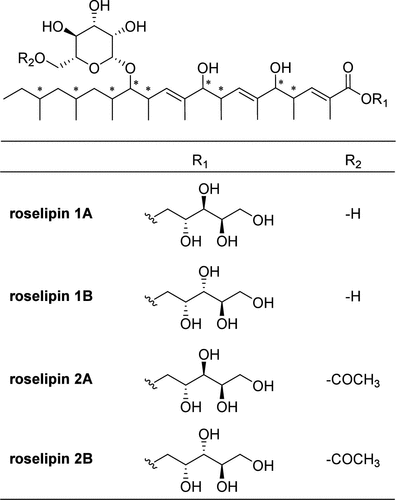
图 1 Roselipins家族分子结构
内容介绍:
研究人员应用此前由该课题组与日本北海道大学的Oikawa课题组合作报道的Biochemistry-based Rule对roselipin 1A结构中聚酮单元9个未确定手性中心的绝对立体化学进行了预测,将roselipin 1A潜在的512种结构缩小至1种,研究人员遂对其预测的结构展开全合成研究,通过立体化学可控的合成策略,最终以最长线性步骤19步,总收率1.77%完成了根据Biochemistry-based Rule预测的roselipin 1A的全合成。最后经过核磁、质谱、旋光等数据的表征并与天然产物roselipin 1A的数据进行比对,其表征数据均高度吻合,证明了由Biochemistry-based Rule预测的结构即为天然产物roselipin 1A的真实立体结构。该工作不仅展现了Biochemistry-based Rule在预测真菌还原型聚酮化合物立体化学方面的准确性,且为此类复杂天然产物的结构鉴定及合成提供指导意义。
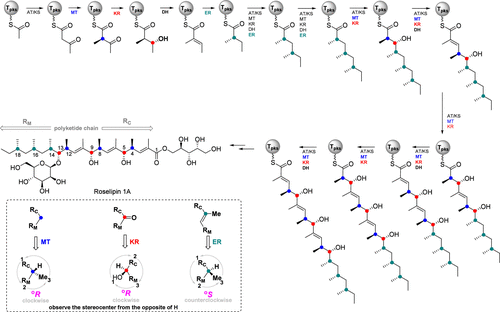
图 2 Roselipin 1A的生源合成途径
叶涛课题组应用Biochemistry-based Rule (与日本北海道大学Oikawa课题组共同提出)对roselipins家族分子结构中聚酮单元9个未确定的手性中心绝对立体化学进行了预测,以roselipin 1A为例,将roselipin 1A潜在的512种结构缩小至1种,得到roselipin 1A的聚酮长链的绝对构型,如图2所示。为了验证该预测规则的准确性以及为了揭示roselipin 1A的真实立体结构,研究人员遂对其预测的结构展开全合成研究。
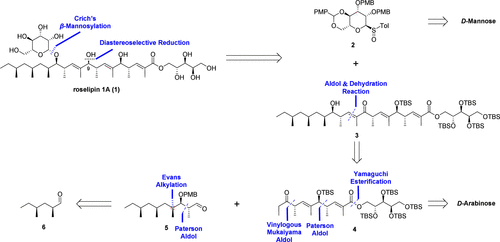
图 3 Roselipin 1A的逆合成分析
Roselipin 1A的逆合成分析如图3所示。Roselipin 1A可以通过后期由Crich课题组开发的 β-Mannosylation及Diastereoselective reduction作为两步关键反应得到,从而可以逆推至糖基亚砜片段2和复杂醇片段3。醇片段3可以由醛5和乙基酮4通过连续的LiHMDS介导syn-aldol和Dehydration elimination作为两步关键反应进行构建。糖基亚砜2、醛5和乙基酮片段4均可以由简单的原料进行制备。
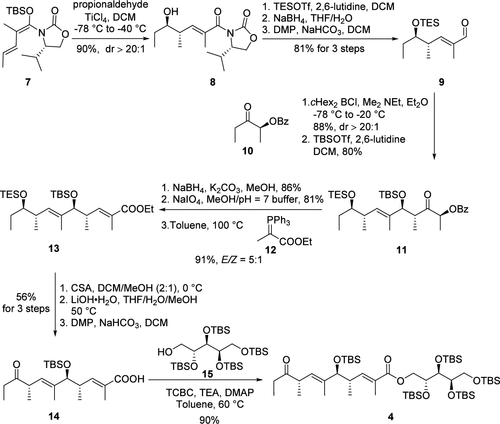
图 4 乙基酮片段4的合成路线
研究人员首先聚焦于右侧乙基酮片段4的合成,合成路线如图4所示。从丙醛出发,经过关键的Vinylogous mukaiyama aldol、Paterson anti aldol、Wittig olefination及简单的官能团转化得到酸14。随后研究人员对酸14和阿拉伯糖醇衍生物15的关键酯化反应进行了条件优化,最终发现在Yamaguchi esterification的条件下,通过将酸14和阿拉伯糖醇衍生物15预先混合的方式及加热至60 ℃的条件下,获得最佳产率为90%,且未观察到对称酸酐副产物的形成。
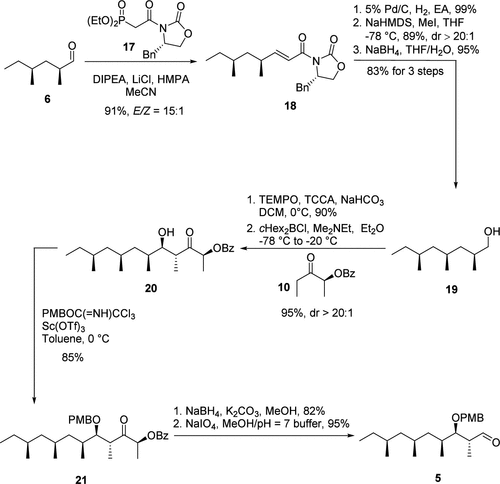
图 5 醛片段5的合成路线
随后研究人员聚焦于左侧醛片段5的合成,合成路线如图5所示。从已知的醛6出发,经过关键的三步连续转化:Horner–Wadsworth–Emmons (HWE) olefination、Hydrogenation及Evans asymmetric methylation。能够以20克规模得到醇片段19。随后醇片段19经过关键Paterson anti aldol及简单的官能团转化得到醛片段5。
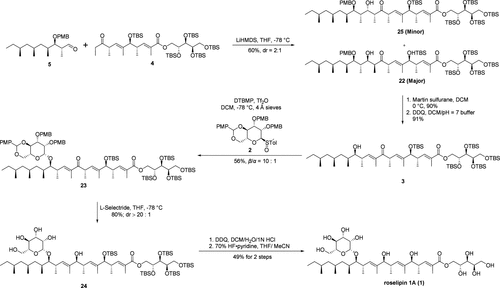
图 6 Roselipin 1A的合成路线
在得到乙基酮片段4和醛片段5之后,研究人员着手于roselipin 1A的最终合成,合成路线如图6所示。研究人员利用LiHMDS介导的syn aldol反应成功将乙基酮片段4和醛片段5进行偶联,两种偶联产物均可以在Martin's sulfurane试剂条件下发生脱水消除反应得到E式α,β-不饱和酮。在获得醇片段3后,研究人员利用Crich课题组开发的 β-Mannosylation反应,以糖基亚砜2作为糖基供体,在标准的糖苷化反应条件下,成功地以α/β为1:10的比例得到β-糖苷化产物23。随后β-糖苷化产物23经过关键的L-Selectride介导的非对映选择性还原,以优异的非对映选择性得到目标产物醇24。随后醇24经过两步脱保护基操作得到roselipin 1A。最后经过核磁、质谱、旋光等数据的表征并与天然产物roselipin 1A的数据进行比对,其表征数据均高度吻合,证明了由Biochemistry-based Rule预测的结构即为天然产物roselipin 1A的真实立体结构。
总结/展望:
叶涛课题组结合Biochemistry-based Rule和全合成成功揭示了糖脂类天然产物roselipin 1A的真实绝对构型。研究人员应用Biochemistry-based Rule对roselipin 1A结构中聚酮单元9个未确定手性中心的绝对立体化学进行了预测,将roselipin 1A潜在的512种结构缩小至1种,随后经全合成验证确定了roselipin 1A的真实立体结构。该工作不仅展现了Biochemistry-based Rule在预测真菌还原型聚酮化合物立体化学方面的准确性,且为此类复杂天然产物的结构鉴定及合成提供指导意义。
Cite this: Jiang, Y.; Liu, J.; Guo, Y.; Ye, T. Total Synthesis and Stereochemical Assignment of Roselipin 1A. Precision Chemistry 2024, 3 (2), 82–88. https://doi.org/10.1021/prechem.4c00082.
