英文原题:Catalytic Reductive Homocoupling of Benzyl Chlorides Enabled by Zirconocene and Photoredox Catalysis
通讯作者:Eisuke Ota,Junichiro Yamaguchi,日本早稻田大学
作者:Ryota Tajima, Keisuke Tanaka, Kazuhiro Aida, Eisuke Ota, Junichiro Yamaguchi
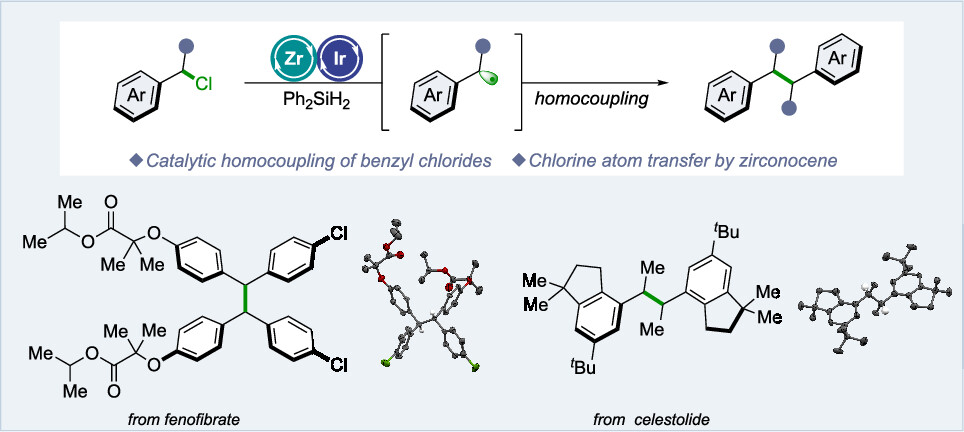
研究背景:
C-C键的高效构建是有机合成化学的核心挑战之一。尽管已经有大量成熟的 C−C 键形成方法,但寻找更简便、高效的构建策略依然是有机合成化学的研究重点。其中,自由基-自由基偶联是形成C(sp³)−C(sp³)键的有效途径。可见光催化技术进一步推动了这一领域的发展,其温和的反应条件和对多种官能团的兼容性使其成为实现C-C键合成的理想手段。苄基卤化物是一类重要的自由基偶联反应前体,但现有的可见光介导的苄基卤化物自由基偶联反应研究主要使用苄基溴作为底物。相比之下,化学稳定性更高且来源更为丰富的苄基氯在此类反应中研究较少。苄基氯的 C-Cl 键断裂需要克服较高的活化能,现有的方法大多依赖于苛刻的反应条件,因此适用范围较为有限。本文针对苄基氯的活化难题,提出了一种基于茂锆和光氧化还原催化协同作用的新策略。在温和条件下,通过茂锆介导的的氯原子转移(XAT)高效生成苄基自由基,实现苄基氯的还原自偶联,进而构建 C(sp³)-C(sp³) 键。这一方法为苄基氯的活化转化提供了新策略,也为复杂分子的合成和功能化提供了新思路。
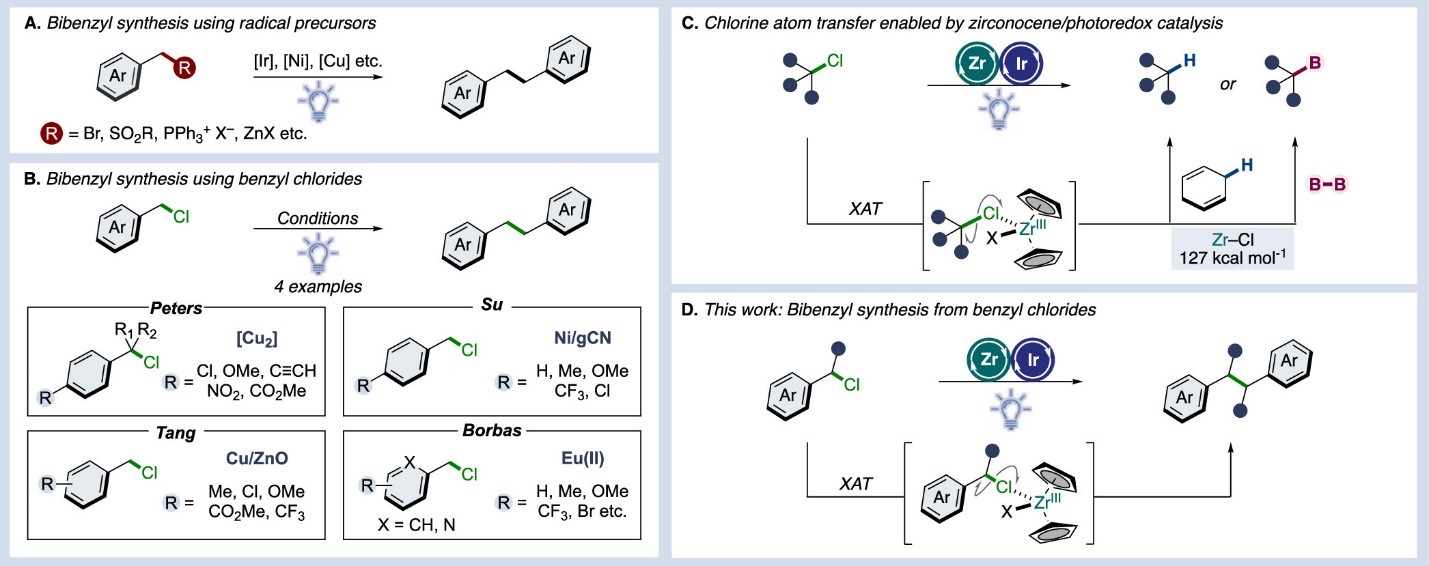
图1 (A)基于自由基前体的二芳基乙烷合成;(B)基于苄基氯的二芳基乙烷合成;(C)茂锆/光氧化还原催化促进的氯原子转移;(D)本研究:基于苄基氯的二芳基乙烷合成
内容介绍:
催化体系设计新颖
茂锆(Cp2ZrCl2)和光催化剂(Ir(4-MeOppy)3)协同作用实现C-Cl键的活化,通过氯原子转移(XAT)机制高效生成苄基自由基,克服了传统强还原条件的局限。氢硅烷(Ph2SiH2)作为反应添加剂,在催化循环中起到了关键作用。
反应机理的深入探讨
通过Stern-Volmer实验、自由基钟实验与产物分析、NMR谱等多种实验验证了苄基自由基的生成和参与过程,揭示了氯原子转移(XAT)机制以及光氧化还原催化与锆茂的协同作用。新机制突破了苄基氯C-Cl键断裂的传统挑战,为自由基化学提供了新策略。
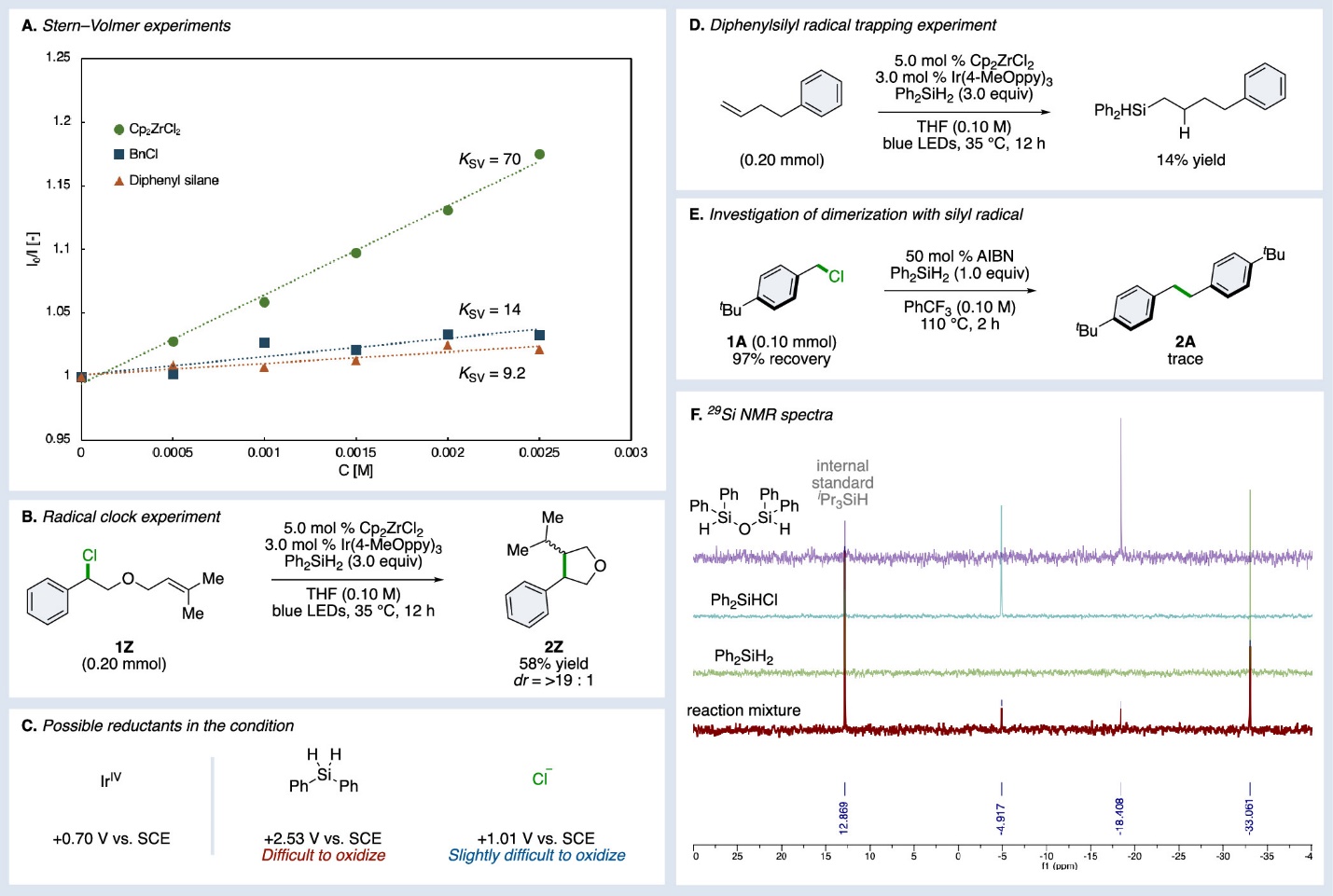
图2 多种实验验证苄基自由基的生成和参与过程
Stern-Volmer实验(图2A)结果表明,相比于苄基氯和二苯基硅烷,茂锆(Cp₂ZrCl₂)对激发态的光催化剂Ir(4-MeOppy)₃具有显著的淬灭作用,支持了氯原子转移机理而非苄基氯的单电子还原机理。自由基钟实验(图2B)表明反应可能经历苄基自由基中间体。图 2C-F 的相关实验进一步探讨了二苯基硅烷在反应中的参与过程和反应途径。。
底物适用范围广
通过全面的底物探索,展现出该方法在不同类型苄基氯衍生物和复杂分子中的广泛应用。反应对烷基、硫化物、腈基、酯基、芳基卤(氟、氯、溴)等多种官能团表现出优异的耐受性。芳杂环底物(吲哚、苯并噻吩、恶唑)也能以高选择性生成目标偶联产物。大位阻底物五甲基苄基氯仍能有效反应,表明位阻对偶联效率影响较小,富电子和缺电子芳环底物均能以较高产率生成目标产物,展现了对底物电子效应的良好适应性。该方法还能成功地应用于药物分子(如非诺贝特和氯吡格雷)衍生物的后期修饰以及活性天然产物 Brittonin A 的高效合成,充分展示了其在药物开发和分子修饰中的广阔潜力和重要价值。
总结/展望:
本文开发了一种基于茂锆与光氧化还原催化协同作用的苄基氯还原自偶联反应策略。该方法不仅对多种官能团表现出优异的耐受性,还可广泛应用于生物活性分子衍生物的自偶联以及天然二芳基乙烷类化合物的高效合成。一系列机理研究阐明了氢硅烷添加剂的作用。目前,基于该策略的更多转化反应研究正在进行中。
Cite this: Tajima, R.; Tanaka, K.; Aida, K.; Ota, E.; Yamaguchi, J. Catalytic Reductive Homocoupling of Benzyl Chlorides Enabled by Zirconocene and Photoredox Catalysis. Precision Chemistry 2024. https://doi.org/10.1021/prechem.4c00077.
